- Författare Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:40.
- Senast ändrad 2025-01-23 12:47.
Korrosion är en process genom vilken järn bryts ned genom närvaron av olika oxidationsmedel i miljön. Korrosion tar många former och kan ha många orsaker. Ett vanligt exempel är rostprocessen, där järn oxiderar i närvaro av fukt. Korrosion är ett allvarligt problem för tillverkare av byggnader, båtar, flygplan, bilar och andra metallprodukter. När till exempel järn används som en del av en bro är järnets strukturella integritet, som kan skadas av korrosion, avgörande för säkerheten för de som använder bron. Se steg 1 nedan för att lära dig hur du skyddar järn mot korrosionshotet och hur du sänker korrosionshastigheten.
Steg
Metod 1 av 3: Förstå vanliga typer av järnkorrosion
Eftersom så många olika typer av järn används idag måste byggare och tillverkare skydda sig mot många typer av korrosion. Varje järn har unika elektrokemiska egenskaper som avgör vilken typ av korrosion (om någon) det är mottagligt för. Tabellen nedan beskriver några vanliga järn och de typer av korrosion de kan genomgå.
| Järn | Sårbarhet i järnkorrosion | Allmänna förebyggande tekniker | Galvanisk aktivitet* |
|---|---|---|---|
| Rostfritt stål (passivt) | Uniform attack, galvanisk, perforerad, sprucken (allt huvudsakligen i havsvatten) | Rengöring, skyddande beläggning eller tätning | Låg (initiala former av korrosion bildar ett skyddande oxidationsskikt) |
| Järn | Uniform attack, galvanisk, spricka | Rengöring, skyddande beläggning eller tätning, galvanisering, rostskydd | Lång |
| Mässing | Uniform attack, dezincification, stress | Rengöring, skyddande beläggning eller tätning (vanligtvis olja eller lack), tillsats av bly, aluminium eller arsenik till legeringar | För närvarande |
| Aluminium | Galvanisk, hål, sprickor | Rengöring, skyddande beläggning eller tätning, anod, galvanisering, katodiskt skydd, elektrisk isolering | Hög (initial korrosion bildar ett motståndskraftigt oxidationsskikt) |
| Koppar | Galvanisk, hål, estetisk fläck | Rengöring, skyddande beläggning eller tätning, tillsats av nickel till metalllegeringar (speciellt för saltlake) | Låg (initial korrosion bildar en kvarvarande patina) |
*Tänk på att kolumnen "Galvanisk aktivitet" refererar till den relaterade kemiska aktiviteten för järn enligt beskrivningen i den galvaniska tabellen för referenskällan. I denna tabell, "ju högre järnets galvaniska aktivitet, desto snabbare kommer den att genomgå galvanisk korrosion i kombination med mindre aktivt järn."

Steg 1. Förhindra enhetlig attackkorrosion genom att skydda järnytan
Enhetlig angreppskorrosion (ibland förkortad till "enhetlig" korrosion) är en typ av korrosion som uppstår följaktligen på ett enhetligt sätt över exponerade metallytor. I denna typ av korrosion angrips hela järnytan av korrosion och korrosionen fortsätter således med en jämn hastighet. Till exempel, om ett oskyddat metalltak regelbundet utsätts för regn, kommer hela takytan att komma i kontakt med samma mängd vatten och därmed korrodera med en jämn hastighet. Det enklaste sättet att skydda mot enhetlig attack är vanligtvis att placera en skyddsbarriär mellan bären och det frätande medlet. Detta kan vara ett antal saker - färg, oljetätningar, "eller" en elektrokemisk lösning, till exempel en galvaniserande zinkbeläggning.
I situationer under jord eller nedsänkning är en katodisk sköld också ett bra alternativ
Steg 2. Förhindra galvanisk korrosion genom att avbryta flödet av joner från ett järn till ett annat
En viktig form av korrosion som kan uppstå oberoende av järnets fysiska styrka är galvanisk korrosion. Galvanisk korrosion uppstår när två järn med olika elektrodpotentialer kommer i kontakt med närvaron av en elektrolyt (t.ex. saltvatten) som skapar en elektrisk ledningsbana mellan dem. När detta händer flyter järnjoner från det mer aktiva järnet till det mindre aktiva järnet, vilket gör att det mer aktiva järnet korroderar snabbare och det mindre aktiva järnet korroderar långsammare. I praktiken betyder detta att korrosion kommer att utvecklas på det mer aktiva järnet vid kontaktpunkten mellan de två järnen.
- Varje skyddsmetod som förhindrar flödet av joner mellan järnen kan stoppa galvanisk korrosion. Att ge järnet ett skyddande lager kan hjälpa till att förhindra att elektrolyter från omgivningen skapar en elektrisk ledningsbana mellan de två järnen, vilket elektrokemiska avskärmningsprocesser som galvanisering och anod också fungerar bra. Du kan också förhindra galvanisk korrosion av elektriskt isolerande järnområden i kontakt.
- Dessutom kan användning av katod- eller anodskydd skydda det viktiga järnet från galvanisk korrosion. Se nedan för mer information.

Steg 3. Förhindra gropkorrosion genom att skydda järnytan, undvika kloridkällor i miljön och undvika hack och repor
Pitting är en form av korrosion som sker i mikroskopisk skala men kan få stora konsekvenser. Hål är ett stort bekymmer för järn som härleder sin korrosionsbeständighet från ett tunt lager av passiv förening på dess yta, eftersom denna form av korrosion kan leda till strukturfel i situationer där en skyddande beläggning normalt skulle förhindra det. Hål uppstår där en liten bit järn tappar sitt passiva skyddande lager. När detta inträffar uppstår galvanisk korrosion i mikroskopisk skala, vilket leder till bildandet av små hål i järnet. I det här hålet blir miljön hög i syra, vilket påskyndar processen. Hål förhindras vanligtvis genom att applicera ett skyddande lager på metallytan och/eller använda katodiskt skydd.
Exponering för en miljö med hög kloridhalt (t.ex. saltvatten) kan påskynda perforeringsprocessen

Steg 4. Förhindra sprickbildning genom att minimera trånga utrymmen i objektets design
Sprickorosion uppstår i metallföremål där utrymme till vätskan (luft eller vätska) är mycket dålig - till exempel under bultar, under brickor, under spindlar eller mellan gångjärnsskarvar. Sprickorosion uppstår där gapet mellan metallytorna är tillräckligt stort för att vätska ska kunna tränga in men tillräckligt smalt så att vätskan är svår att fly och blir stillastående. Miljön i detta lilla utrymme blir frätande och järnet börjar korrodera i en process som liknar sprickorrosion. Förhindra korrosionssprickor är i allmänhet ett designproblem. Genom att minimera förekomsten av smala luckor i konstruktionen av metallföremål genom att täcka dessa luckor eller ge cirkulation, är det möjligt att minimera sprickkorrosion.
Sprickkorrosion är ett särskilt bekymmer vid hantering av järn, t.ex. aluminium, som har ett passivt yttre skyddande skikt, eftersom sprickkorrosionsmekanismer kan bidra till nedbrytning av denna beläggning

Steg 5. Förhindra spänningskorrosion genom att endast använda säkra laster och/eller glödgning
Spänningskorrosionssprickor (SCC) är en form av korrosionsrelaterat konstruktionsfel som oroar ingenjörer som konstruerar byggnadsstrukturer som stöder kritiska belastningar. Med förekomsten av SCC bildar järnet som stöder lasten sprickor och sprickor under dess lastgräns - i allvarliga fall, i mindre utsträckning. I närvaro av frätande joner sprids mikroskopiska små sprickor i järnet som orsakas av dragspänningen hos de tunga laddningarna när de frätande jonerna når sprickans spets. Detta gör att sprickan långsamt förstoras och kan leda till strukturellt misslyckande. SCC är särskilt farligt eftersom det kan förekomma även i närvaro av material som i allmänhet är mindre frätande för järn. Detta innebär att denna skadliga korrosion uppstår medan resten av järnytan verkar opåverkad.
- Att förebygga SCC är delvis ett designproblem. Exempelvis kan val av material som är SCC -resistenta i den miljö där järnet fungerar och se till att järnmaterialet är korrekt stresstestat hjälpa till att förhindra SCC. Dessutom kan processen med att stärka järnet avlägsna kvarvarande spänningar från konstruktionen.
- SCC har varit känt för att förvärras av höga temperaturer och närvaron av lösta kloridinnehållande vätskor.
Metod 2 av 3: Förhindra korrosion med hemlösningar

Steg 1. Måla järnytan
Kanske den vanligaste och billigaste metoden för att skydda järn mot korrosion är att helt enkelt täcka det med ett lager färg. Korrosionsprocessen innebär att fukt och oxidationsmedel interagerar med järnytan. På det sättet, om järnet är belagt med en skyddande färgspärr, kan varken fukt eller oxidationsmedel komma i kontakt med själva järnet och korrosion uppstår inte.
- Själva färgen är emellertid utsatt för nedbrytning. Måla om när något är flisat, slitet eller skadat. Om färgen försämras så att järnet exponeras, var noga med att inspektera för korrosion eller skador på det utsatta järnet.
-
Det finns många metoder för att måla metallytor. Metallarbetare använder ofta flera av dessa metoder för att säkerställa att alla metallföremål får en noggrann beläggning. Nedan följer några exempel på metoder med kommentarer om deras användning:
- Borste - används för svåråtkomliga utrymmen.
- Rulle - används för att täcka stora utrymmen. Billigt och enkelt.
- Luftspray - används för att täcka stora utrymmen. Snabbare men inte lika lätt som en rulle (slöseri med färg).
- Airless spray/elektrostatisk airless spray - används för att täcka stora utrymmen. Snabb och tillåter varierande grader av tjock/tunn konsistens. Inte så slöseri som vanligt sprayvatten. Utrustning är ganska dyr.

Steg 2. Använd marint färg för vatten som utsätts för järn
Metallföremål som regelbundet (eller ständigt) kommer i kontakt med vatten, som båtar, kräver speciell färg för att skydda mot den höga sannolikheten för korrosion. I denna situation är "normal" korrosion i form av rostning inte det enda problemet (även om det är ganska stort), eftersom marint liv (havskulor, etc.) kan växa på oskyddat järn som kan vara en källa till slitage och ytterligare korrosion. För att skydda metallföremål som båtar och andra, var noga med att använda en högkvalitativ epoxy marin färg. Denna typ av färg skyddar inte bara järnet från fukt, utan förhindrar också tillväxten av marint liv på dess yta.
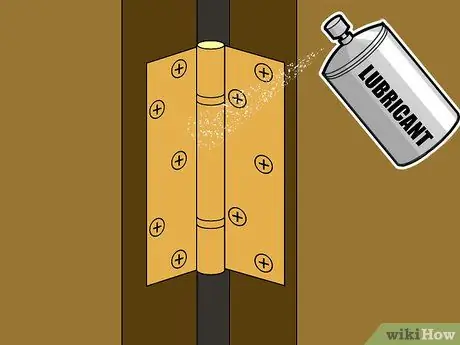
Steg 3. Applicera skyddande smörjning på rörliga metalldelar
För platta och statiska metallytor gör färg ett utmärkt jobb med att hålla fukt borta och förhindra korrosion utan att påverka järnets användbarhet. Färg är dock vanligtvis inte lämplig för rörliga metalldelar. Till exempel, om du målar på ett dörrgångjärn, när färgen torkar, håller den gångjärnet och blockerar dess rörelse. Om du tvingar dörren att öppna, kommer färgen att spricka och lämnar utrymme för fukt att nå järnet. Ett bättre val för järnhaltiga delar som gångjärn, skarvar, axlar och så vidare är en lämplig vattenolöslig smörjning. Detta grundliga lager smörjmedel kommer att avvisa fukt samtidigt som det säkerställer smidig och enkel rörelse av dina metalldelar.
Eftersom smörjmedel inte torkar på plats som färg, kan de försämras med tiden och kräver regelbunden återanvändning. Applicera regelbundet smörjning på metalldelar för att säkerställa att de förblir effektiva som en skyddande tätning

Steg 4. Rengör metallytan noggrant innan målning eller smörjning
Oavsett om du använder vanlig färg, marinfärg eller skyddande smörjning/tätning, bör du se till att ditt strykjärn är rent och torrt innan appliceringsprocessen påbörjas. Se till att järnet är fritt från befintlig smuts, fett, svetsrester eller korrosion, eftersom det kan slösa din ansträngning genom att bidra till korrosion i framtiden.
- Jord, olja och annat skräp kan störa färg och smörjning genom att förhindra att färgen eller smörjmedlet fastnar direkt på metallytan. Till exempel, om du målar på en stålplåt med ett järnskrot ovanpå, torkar färgen ovanpå slipningen och lämnar tomt utrymme i järnet under. Om och när sliparen faller. Den exponerade delen är känslig för korrosion.
- Om du målar eller smörjer en järnyta med befintlig korrosion bör ditt mål vara att göra ytan så slät och normal som möjligt för att säkerställa bästa möjliga tätningsvidhäftning till järnet. Använd en borste, sandpapper och/eller kemisk rostborttagare för att avlägsna så mycket korrosion som möjligt.

Steg 5. Håll oskyddade järnprodukter borta från fukt
Som nämnts ovan förvärras de flesta former av korrosion av fukt. Om du inte kan applicera ett skyddande lager med färg eller tätning på ditt strykjärn bör du vara försiktig så att det inte utsätts för fukt. Att anstränga sig för att hålla oskyddade järnverktyg torra kan öka deras användbarhet och förlänga deras effektiva livslängd. Om ditt strykjärn utsätts för vatten eller fukt, var noga med att rengöra och torka det direkt efter användning för att förhindra att korrosion startar.
Förutom att övervaka exponeringen för fukt under användning, se till att förvara metallföremål inomhus, på en ren och torr plats. För stora föremål som inte passar i ett skåp eller skåp, täck föremålet med en trasa. Detta hjälper till att avvisa fukt från luften och förhindrar att damm samlas på ytan

Steg 6. Se till att metallytan är så ren som möjligt
Efter varje användning av ett metallföremål, oavsett om metallen är målad eller inte, se till att rengöra dess funktionella yta, ta bort smuts, fett eller damm. Ansamling av smuts på metallytan kan bidra till slitage av järnet och/eller dess skyddande beläggning, vilket kan leda till korrosion över tiden.
Metod 3 av 3: Förhindra korrosion med avancerade elektrokemiska lösningar
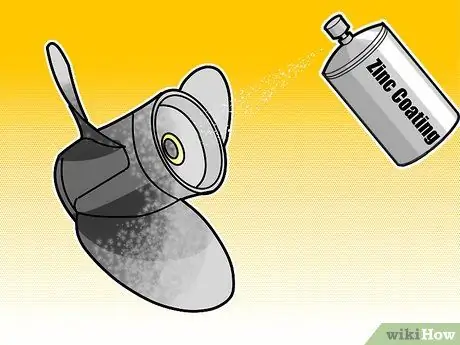
Steg 1. Använd galvaniseringsprocessen
Galvaniserat järn är järn som har belagts med ett tunt lager zink för att skydda det mot korrosion. Zink är mer kemiskt aktivt än det underliggande järnet, så det oxiderar när det utsätts för luft. När zinkskiktet oxiderats bildar det ett skyddande skikt som förhindrar ytterligare korrosion av det underliggande järnet. Den vanligaste typen av galvanisering idag är en process som kallas varmförzinkning där en järnbit (vanligtvis stål) sänks ned i varmt smält zink för att få en enhetlig beläggning.
-
Denna process innefattar hantering av industrikemikalier, varav några är farliga vid rumstemperatur, vid mycket höga temperaturer och bör inte försökas av någon annan än en utbildad professionell. Nedan följer de grundläggande stegen i varmförzinkningsprocessen för stål:
- Stålet rengörs med en het lösning för att avlägsna smuts, olja, färg, etc., sköljs sedan noggrant.
- Stål sänks ned i syra för att avlägsna kvarnskalan och sköljs sedan.
- Ett material som kallas”fluss” appliceras på stålet och får torka. Detta hjälper det sista zinkskiktet att fästa vid stålet.
- Stålet sänks ned i varmt zink och får nå zinktemperaturen.
- Stålet kyls i en "kyltank" fylld med vatten.

Steg 2. Använd offeranoden
Ett sätt att skydda järnföremål från korrosion är att elektriskt fästa en liten, reaktiv metall som kallas en "offeranod" till den. På grund av det elektrokemiska förhållandet mellan den större järnkroppen och den lilla reaktiva kroppen (som beskrivs kortfattat nedan) kommer endast det lilla och reaktiva järnet att genomgå korrosion och lämna det stora och viktiga järnet intakt. När offeranoden korroderar helt måste den bytas ut annars korroderar det större järnet. Denna metod för korrosionsskydd används vanligtvis för nedgrävda strukturer som underjordiska lagertankar eller föremål som är i konstant kontakt med vatten, till exempel båtar.
- Offeranoden är gjord av flera olika typer av reaktivt järn. Zink, aluminium och magnesium är de tre vanligaste järnen som används för detta ändamål. På grund av de kemiska egenskaperna hos dessa material används zink och aluminium vanligen för järnhaltiga material i saltvatten, medan magnesium är mer lämpligt för sötvattenändamål.
- Offeranoder kan användas på grund av den kemiska processen för korrosion i sig. När ett järnföremål korroderar bildas naturligt områden som är kemiskt lik anoden och katoden i en elektrokemisk cell. Elektroner flyter från anoden vid järnytan till den omgivande elektrolyten. Eftersom offeranoden är mycket reaktiv jämfört med järnet som skyddas, blir själva föremålet i hög grad katodiskt genom jämförelse och således flyter elektroner ut ur offeranoden, vilket får det att korrodera men inte resten av järnet.

Steg 3. Använd”imponerad ström”
Eftersom den elektrokemiska processen bakom korrosion av järn involverar flödet av elektricitet i form av elektroner som strömmar ut ur järnet, är det möjligt att använda en extern elektrisk strömkälla för att kontrollera det frätande flödet och förhindra korrosion. Denna process (kallad "imponerad ström") är en kontinuerlig negativ järnladdning på det skyddade järnet. Denna laddning överväldigar flödet som får elektroner att flöda ut ur järnet, vilket förhindrar korrosion. Denna typ av skydd används vanligtvis för nedgrävda järnkonstruktioner som lagringstankar och rör.
- Var medveten om att den typ av elektrisk ström som används för skyddade system för imponerande ström oftast är likström (DC).
- Normalt genereras en imponerad ström som förhindrar korrosion genom att begrava två järnanoder i marken nära ett skyddat metallföremål. Elektrisk ström sänds genom isoleringstråden vid anoden, som sedan rinner genom marken och in i metallföremålet. Elektricitet flyter genom järnföremål och återgår sedan till elkällan (generatorer, likriktare, etc.) genom isoleringstrådar.

Steg 4. Använd anodisering
Anodisering är ett speciellt ytskyddsskikt som används för att skydda järn mot korrosion. Om du någonsin har sett en ljusfärgad järnkarbin har du sett en färgad anodiserad järnyta. I stället för att involvera den fysiska appliceringen av en skyddande beläggning, såsom färg, använder anodisering en elektrisk ström för att ge järnet ett skyddande lager som förhindrar nästan alla former av korrosion.
- Den kemiska processen bakom anodisering innebär att många järn, som aluminium, naturligt bildar kemiska produkter som kallas oxider när de kommer i kontakt med syre i luften. Detta resulterar i att järnet normalt har ett tunt yttre oxidskikt som skyddar (i varierande grad, beroende på järnet) mot ytterligare korrosion. Den elektriska ström som används i anodiseringsprocessen skapar vanligtvis en tjockare byggnad av denna oxid på järnets yta än vanligt, vilket ger stort skydd mot korrosion.
-
Det finns flera olika sätt att donera järn. Nedan följer de grundläggande stegen i en av anodiseringsprocesserna. Se Hur man anodiserar aluminium för mer information.
- Aluminium rengörs och avoljas.
- Föroreningar på aluminiumytan avlägsnas med en smutslösning.
- Aluminiumet placeras i ett syrabad vid konstant ström och temperatur (till exempel 12 ampere/kvadratfot och 70-72 grader F (21-22 grader C).
- Aluminium avlägsnas och sköljs.
- Aluminium införs valfritt i färgämnet vid 38-60 grader C (100-140 grader F).
- Aluminium förseglas genom att sänka det i kokande vatten i 20-30 minuter.

Steg 5. Använd passivt järn
Som nämnts ovan bildar en del järn naturligt ett skyddande oxidskikt när det utsätts för luft. En del järn bildar detta oxidlager så effektivt att det blir kemiskt inaktivt. Vi säger att järn är "passivt" med hänvisning till en "passiv" process där det blir mindre reaktivt. Beroende på användningen kanske passiva järnföremål inte behöver "extra" skydd för att göra dem korrosionsbeständiga.
-
Ett välkänt exempel på passivt järn är rostfritt stål. Rostfritt stål är en vanlig legering av stål och krom som motstår korrosion under de flesta förhållanden utan att kräva skydd. För de flesta dagliga användningsområden är korrosion vanligtvis inte ett problem med rostfritt stål.
Det måste dock sägas att rostfritt stål under vissa förhållanden inte är 100% korrosionsbeständigt - till exempel i saltvatten. På samma sätt blir många passiva strykjärn icke-passiva under extrema väderförhållanden och är därför inte lämpliga för alla applikationer
Tips
- Var medveten om korrosion mellan granuler. Detta påverkar järnets förmåga att formas eller manipuleras och minskar järnets totala styrka.
- American Boat and Yacht Council rekommenderar i allmänhet att binda båten. Båtar av aluminium och stål bör dock inte spännas fast för att förhindra att järnet korroderar.
Varning
- Lämna aldrig starkt korroderade metalldelar i fordon eller båtar. Graden av korrosion varierar, men eventuell korrosion kan tyda på allvarliga strukturella skador. För säkerhets skull, byt ut eller ta bort alla tecken på järnkorrosion.
- Måla inte den när du använder en offeranod. Det skulle göra det omöjligt för elektroner att passera in i omgivningen och ta bort dess korrosionshindrande kraft.






